
Click-iT 647 Tunel Cell Apoptosis Detection Kit
- 50 T
产品信息
产品名称 | 产品编号 | 规格 |
Click-iT 647 Tunel Cell Apoptosis Detection Kit | G1509-50T | 50T |
产品描述
细胞凋亡中染色体DNA的断裂是个渐进的阶段性过程。染色体DNA首先在内源性的核酸水解酶的作用下降解为50-300 kb的大片段,然后大约30%的染色体DNA在Ca2+和Mg2+依赖的核酸内切酶作用下,在核小体单位之间被随机切断,形成180-200 bp核小体DNA多聚体。因此在细胞凋亡晚期,DNA会被降解为180-200 bp的片段,断裂的基因组DNA上暴露出大量的3'-OH末端。末端脱氧核糖核苷酸转移酶(Terminal Deoxynucleotidyl Transferase, TdT)是一种不依赖于模板的DNA聚合酶,可以催化脱氧核苷酸结合到断裂的DNA分子3'-OH末端。因此TUNEL (TdT mediated dUTP Nick End Labeling)细胞凋亡检测试剂盒可以用来检测组织细胞在凋亡晚期过程中细胞核DNA的断裂情况。
其原理是在TdT酶的作用下,在基因组DNA断裂时暴露出的3´-OH末端掺入EdUTP(一种带有炔烃修饰的dUTP),炔烃基团在一价铜离子催化下与叠氮染料发生成环反应(点击反应)从而定点引入荧光基团,本试剂盒使用的是iF647 azide,从而可以用荧光或共聚焦显微镜检测(iF647激发656 nm,发射670 nm)。相比较于其它修饰的dUTP,EdUTP有更小的空间位阻,更容易被TdT酶掺入到DNA末端。
本试剂盒应用范围广,适用于石蜡组织切片,冰冻组织切片、细胞爬片、细胞涂片等的细胞凋亡检测。
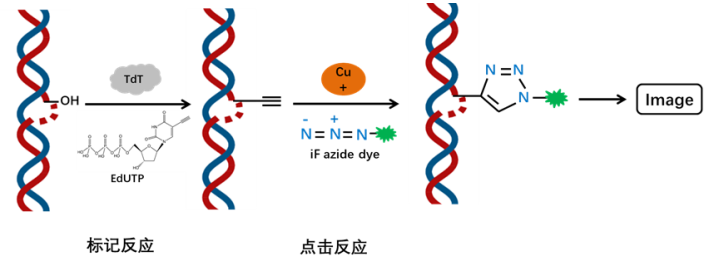
图1. 基于点击化学TUNEL试剂盒原理示意图
储存与运输
冰袋(wet ice)运输;-20℃存储,有效期12个月。
组成
Component Number | Component | G1509-50T |
G1509-1 | Recombinant TdT Enzyme | 100 µL |
G1509-2 | EdUTP Labeling Mix | 250 µL |
G1509-3 | Equilibration Buffer | 5×1 mL |
G1509-4 | Proteinase K(200 µg/mL) | 1 mL |
G1509-5 | iF647 azide dye | 80 μL |
G1509-6 | Reaction Buffer A | 5×1 mL |
G1509-7 | Reaction Buffer B | 60 μL |
G1509-8 | Reaction additive(Reagent C) | 2×100 mg |
产品说明书 | 1份 | |
实验前准备
2. 固定液:溶于PBS的4%多聚甲醛,pH 7.4(推荐G1101);
3. 破膜液:溶于0.1%柠檬酸钠的0.1% Triton X-100(推荐G1204);
4. PBS配制的0.2%的Triton X-100;PBS配制的0.1%的Triton X-100,其中含5 mg/mL BSA;
5. 如需染核,需自备DAPI(2 µg/mL)、Hoechst 33258或PI(1 µg/mL)(推荐G1012、G1011、G1021);
6. 如需阳性对照实验,需自备DNase I(推荐G3342)
7. Reaction additive(Reagent C)低速离心,100 mg粉末中加入1 mL超纯水溶解(即可使用),并100 μL分装后于-20℃存储,剩余粉末留作备用;(Reagent C易氧化,尽量避免长时间暴露于空气中,配成水溶液后强烈建议分装成小份使用;经测试Reagent C水溶液颜色发生轻微变化,点击反应体系依然可以正常进行,如呈现棕色,表明该组份已经失效)
8. 如果结果背景颜色过深,可能是实验过程中洗涤不充分、固定液残留导致;
9. 点击反应液体系注意要按照顺序进行依次添加,边加边混匀;
10. 为了您的安全和健康,请穿实验服并戴一次性手套操作。
操作步骤
一、样品准备
A. 石蜡包埋组织切片
1. 室温下将石蜡组织切片放入环保型脱蜡透明液(G1128)中浸泡5-10 min,重复3次;然后无水乙醇浸泡5 min,重复2次;最后用梯度乙醇(85%、75%、双蒸水)各浸泡1次,每次5 min;
2. 用PBS轻轻润洗切片,并去掉样本周围多余液体,使用组化笔沿组织外围轮廓画一个与组织间隔2-3 mm的小圈,便于下游通透性处理和平衡标记操作,在实验过程中,切勿让样品干燥,处理好的样本放在湿盒中保持样本的湿润;
3. 配制Proteinase K工作液:按1:9的比例,用PBS作为稀释液来稀释Proteinase K(200 µg/mL)原液,使其终浓度为20 μg/mL;
4. 每个样本上滴加100 μL上述Proteinase K工作液,使其被全部覆盖,37℃孵育20 min;
(注:Proteinase K处理主要有助于组织和细胞后续步骤的染色试剂通透,其孵育时间过长过短都会影响后续标记效率,为得到更好的结果,可以根据实际情况优化孵育时间)
5. 用PBS溶液浸润清洗样本3次,每次5 min(Proteinase K需洗涤干净,否则会干扰后续的标记反应)。处理后的样本放在湿盒中保持样本的湿润;
6. (可选步骤)去掉样本上多余的液体,将适量破膜液滴加到组织上,充分浸润组织,室温处理20 min;破膜处理完成后同样的用PBS溶液润洗样本3次,每次5 min;处理后的样本放在湿盒中保持样本的湿润。
B. 组织冰冻切片
1. 将组织冰冻切片浸没在固定液中,室温孵育固定10-15 min;
2. 将组织切片从固定液中取出,置于通风橱中自然晾干;
3. 将组织切片放入纯水或PBS中润洗,去掉样本上残存的固定液;
4. 用组化笔沿着组织外围轮廓画一个与组织间隔2-3 mm的小圈,便于下游通透性处理和平衡标记操作;在实验过程中,切勿让样品干燥,处理好的样本放在湿盒中保持样本的湿润;
5. 配制Proteinase K工作液:按1:9的比例,用PBS作为稀释液来稀释Proteinase K(200 µg/mL)原液,使其终浓度为20 μg/mL;
6. 每个样本上滴加100 μL上述Proteinase K工作液,使其被全部覆盖,室温孵育10 min;
(注:Proteinase K处理主要有助于组织和细胞后续步骤的染色试剂通透。其孵育时间过长过短都会影响后续标记效率;为得到更好的结果,可以根据实际情况优化孵育时间)
7. 用PBS溶液润洗样本2-3次,去掉多余液体(Proteinase K需洗涤干净,否则会干扰后续的标记反应),处理后的样本放在湿盒中保持样本的湿润;
8. (可选步骤)将适量破膜液滴加到组织上,充分浸润组织,室温处理20 min,破膜处理完成后同样的用PBS溶液润洗样本,去掉多余液体,处理后的样本放在湿盒中保持样本的湿润。
C. 细胞爬片
1. 在Lab-Tek载玻片小室(Chamber Slides)上培养贴壁细胞,在凋亡诱导处理之后,用PBS轻轻润洗2遍载玻片;
2. 向每个载玻片小室中加入适量的固定液覆盖组织,室温下孵育20 min;
3. 去掉固定液,加入PBS清洗3次,每次5 min;
4. 每个样本浸于0.2%配制于PBS中的Triton X-100溶液中,室温孵育5 min进行通透处理;
5. 在盛有PBS溶液的敞口烧杯中浸没清洗样本2-3次;
6. 轻轻去掉多余液体,并用滤纸小心吸干载玻片上样本周围的液体。处理后的样本放在湿盒中保持样本的湿润。
D. 细胞涂片
1. 以约2×107个细胞/mL的浓度将细胞重悬于PBS中,吸取50-100 μL细胞悬液滴于防脱玻片上,使用一片洁净的载玻片轻柔涂开细胞悬液;
2. 将细胞涂片浸入装有固定液的染色缸中,固定细胞,在4℃放置25 min;
3. 将玻片浸入PBS中,室温放置5 min浸洗,重复一次;
4. 轻轻去掉多余液体,并用滤纸小心吸干玻片上样本周围多余的液体,用组化笔沿着细胞外围轮廓画一个小圈,便于下游透性处理和平衡标记操作,在实验过程中,切勿让样品干燥;
5. 每个样本浸于0.2%配制于PBS中的Triton X-100溶液中,室温孵育5 min进行通透处理;
6. 在盛有PBS溶液的敞口烧杯中浸没清洗样本2-3次;
7. 轻轻去掉多余液体,并用滤纸小心吸干载玻片上样本周围的液体。处理后的样本放在湿盒中保持样本的湿润。
二、DNase I处理阳性对照实验(可选步骤)
在样本通透处理后,用DNase I(推荐G3342)处理样本来准备阳性对照。
1. 将100 μL 1×DNase I Buffer(配制方法:取10 μL 10×DNase I Buffer,然后加入90 μL去离子水混匀)滴加到已通透的样本上,室温孵育5 min;
2. 轻轻去掉多余液体,加入100 μL含有DNase I(20 U/mL)的工作液,室温孵育10 min;
3. 轻轻去掉多余的液体,并将载玻片在装有PBS的染色缸中彻底洗3-4次。
(注:阳性对照载玻片必须使用单独的染色缸,否则阳性对照载玻片上残留的DNase I可能会在实验载玻片上引入高背景)
三、标记与检测
1. 平衡:每个样本滴加50 μL Equilibration Buffer使其全部覆盖待检样本区域,室温孵育10 min;
2. 标记液配制:在冰上解冻EdUTP Labeling Mix和Equilibration Buffer,并按照Recombinant TdT enzyme:EdUTP Labeling Mix:Equilibration Buffer=2 µL:5 µL:50 µL(2:5:50)比例混合足够用于所有实验的TdT孵育缓冲液,具体实验使用试剂的体积可以根据玻片的大小进行适当等比例调整;
3. 阴性对照体系:准备一份不含Recombinant TdT enzyme的对照TdT孵育缓冲液,用ddH2O替代;
4. 标记:尽量去掉平衡的Equilibration Buffer,然后在每份组织样本上加入57 μL TdT孵育缓冲液,在37℃孵育1 h;注意不能干片;
5. 立即用PBS润洗组织样本,清洗4次,每次5 min;
6. 点击反应:去掉上一步PBS缓冲液,在样本上滴加100 μL点击反应液,使其全部覆盖样本,室温避光孵育30 min;(点击反应液体系参考下表,依次加入各个试剂,边加边混匀,可等比例增加或减少配制量,建议事先配制)
Component | Volume |
Reaction Buffer A | 925 μL |
Reaction Buffer B | 10 μL |
iF647 azide dye | 15 μL |
Reaction additive(Reagent C) | 50 μL |
总体积 | 1000 μL |
7. 去除点击反应液,立即用PBS缓冲液洗涤2-3次,每次5 min;
8. 用滤纸轻轻擦掉样本周围的PBS溶液;
9. 核染色:样本在染色缸中染色,在黑暗中将载玻片浸入装有DAPI溶液(用PBS新鲜配制并稀释)的染色缸,室温放置8 min(或用Hoechst 33258进行核染色);
10. 封片:样本染色完成后,用PBS清洗组织样本3次,每次5 min,然后轻轻去掉多余液体,滴加抗荧光淬灭封片剂(推荐G1401)封片;
11. 镜检:立即在荧光显微镜下分析样本,载玻片注意避光,DAPI能将凋亡和未凋亡的细胞都染成蓝色,只在凋亡的细胞核中才有iF647 azide dye掺入而定位的粉色荧光。
四、实验流程简图
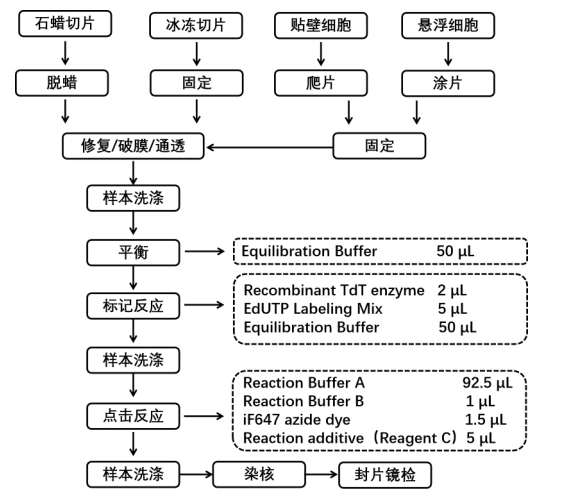
本产品仅供科研用途,不用于临床诊断!
(产品包装升级中,以实物为准。)
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|

