Annexin V法
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|---|---|---|---|
| Y1418-25ML | 抗荧光淬灭封片剂(含DAPI) | 25 mL | 300 | |
| Y6111 | 免疫组化笔(Liquid Blocker PAP Pen) | 支 | 240 | |
| Y6023-1 | 粘附载玻片(石蜡切片) | 50片/盒 | 45 | |
| Y6023-2 | 粘附载玻片(冰冻切片) | 50片/盒 | 45 | |
| Y6028-20 | 粘附载玻片(石蜡切片)(特规大玻片) | 20片/盒 | 100 | |
| Y6069-20 | 粘附载玻片(冰冻切片)(特规大玻片) | 20片/盒 | 100 | |
| Y1215-100ML | 破膜液 | 100 mL | 30 | |
| Y1138-1ML | Hoechst 33342染色液(1 mg/mL) | 1 mL | 150 | |
| Y1022-10ML | Hoechst 33258染液(即用型) | 10 mL | 45 | |
| Y1032-10ML | PI染液 | 10 mL | 45 | |
| YC204014-100ml | 曲拉通X-100(Triton X-100) | 100 mL | 24 |
实验简介
细胞凋亡是发生在胚胎发育和维持组织稳定过程中的正常生理过程,伴随着许多形态学特征改变,其中细胞膜的丢失是细胞凋亡早期的特征之一,在正常细胞中,磷脂酰丝氨酸(phosphotidylserine,PS)只分布在细胞膜磷脂双分子层的内侧,但在细胞凋亡早期,PS会从脂膜的内侧翻转外侧,使其暴露于细胞外侧。Annexin V(膜联蛋白V)是一种Ca2+依赖的磷脂结合蛋白,对PS具有高度亲和力,会与暴露PS的细胞特异性结合,因此Annexin V被作为检测细胞早期凋亡的指标之一。碘化丙啶(Propidium Iodide,PI)是一种核酸染料,它不能透过具有完整细胞膜的正常细胞和早期凋亡细胞,但能透过凋亡晚期和坏死细胞的细胞膜并将细胞核染色。本产品通过将Annexin V用荧光染料分子进行标记后作为检测探针,检测细胞的早期凋亡。同时以PI区分存活的细胞与坏死、晚期凋亡细胞。Annexin V-I荧光染料分子和PI结合使用,活细胞呈现阴性染色(Annexin V-/PI-),早期凋亡细胞呈现单荧光阳性(Annexin V+/PI-),而晚期凋亡细胞和坏死细胞呈现双荧光阳性(Annexin V+/PI+)。本试剂盒适用于流式细胞仪或荧光显微镜检测。
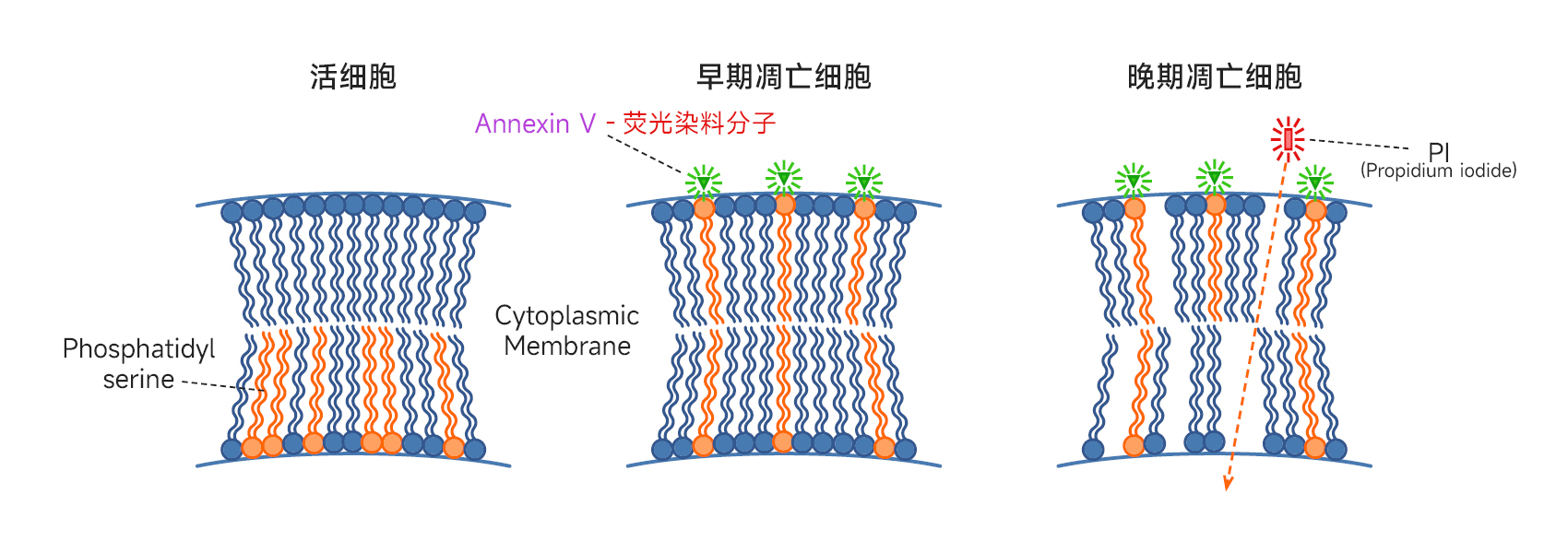
Annexin V法 试剂盒主要成分及用途
| (G1510 EGFP/PI、G1511 FITC/PI、G1512 PE/7-AAD、G1513 IF488/PI、G1514 IF647/PI) | |
| Annexin V-荧光素(EGFP/FITC/PE/IF488/F647) | Annexin V能够与细胞膜外侧暴露的PS高亲和力结合,荧光素可通过荧光显微镜或流式细胞仪观察,从而实现对细胞早期凋亡的检测和定量分析。 |
| PI/7-AAD | 核酸染料,能够与DNA结合发出荧光信号 |
| 1×Binding Buffer | 反应缓冲液,提供适宜的反应环境 |
实验前准备
荧光淬灭封片剂(推荐G1401);
粘附载玻片(推荐:G6012-1、G6012-2、G6017-20、G6058-20,经过粘附处理,能有效防止组织切片脱落)
整个实验过程操作应尽量轻柔避免细胞破碎,影响实验结果。
使用胰酶消化细胞时,应小心操作,避免人为损伤细胞,并控制消化时间。消化时间过短,细胞需用力吹打才能脱落,容易造成细胞膜的机械损伤;若消化时间过长,细胞膜同样容易受到损伤。影响检测结果。另外不能使用含EDTA的胰酶,EDTA会影响Annexin V与PS的结合。
贴壁细胞经凋亡刺激后,如有部分细胞漂浮,需同时收集细胞培养上清液及贴壁细胞合并染色,会使得结果更加准确。
Annexin V-EGFP和PI对光敏感,操作时注意避光。反应结束后应尽快进行检测。
实验过程中请穿实验服并戴一次性手套,避免污染,确保安全。
操作步骤
悬浮细胞:取细胞悬液,经500 g,4℃离心5 min收集细胞;
贴壁细胞:先收集细胞培养上清液。然后用不含EDTA的胰酶(推荐G4002或G4011)消化后,与细胞培养上清液合并,经500 g,4℃离心5 min收集细胞。胰酶消化时间不宜过长,以免过度消化引起假阳性。
重悬细胞:用预冷的1×Binding Buffer轻柔重悬细胞,调整细胞浓度至1~5×106/mL;
染色:取100 μL细胞悬液,按照下表加入对应试剂,轻柔混匀,室温避光8-10 min;
不同试剂盒加入对应的组分 G1510 5 µL Annexin V-EGFP和5 µL PI G1511 5 µL Annexin V-FITC和5 µL PI G1512 5 µL Annexin V-PE和5 µL 7-AAD G1513 5 µL Annexin V-IF488和5 µL PI G1514 5 µL Annexin V-IF647和5 µL PI 检测:加入400 µL预冷的1×Binding Buffer,轻轻摇匀,1 h内用流式细胞仪或者荧光显微镜进行检测。
结果分析
流式细胞仪检测
a.流式细胞仪检测分析时选择合适的电压并调好光补偿
试剂盒货号 建议 G1510 除实验组外建议设置阴性对照(不加任何标记物)用于调节电压,单标对照(只加Annexin V-EGFP,以及只加PI的细胞)用于调节补偿; G1511 除实验组外建议设置阴性对照(不加任何标记物)用于调节电压,单标对照(只加Annexin V-FITC,以及只加PI的细胞)用于调节补偿;; G1512 除实验组外建议设置阴性对照(不加任何标记物)用于调节电压、单标对照(只加Annexin V-PE和只加7-AAD)用于调节补偿; G1513 除实验组外建议设置阴性对照(不加任何标记物)用于调节电压,单标对照(只加Annexin V-IF488和只加PI)用于调节补偿; G1514 除实验组外建议设置阴性对照(不加任何标记物)用于调节电压、单标对照(只加Annexin V-IF647和只加PI)用于调节补偿; b. 流式细胞仪检测分析参考实例:
用5 µM Camptothecin诱导Jurkat T淋巴瘤细胞6 h,参照以上实验步骤,用流式细胞仪进行检测,结果如下图所示。
试剂盒货号 G1510 G1511 G1513 G1514 G1512 横坐标 荧光染料 EGFP FITC IF488 IF647 PE 最大激发波长 488 nm 488 nm 491 nm 656 nm 565 nm 最大发射波长 507 nm 525 nm 518 nm 670 nm 578 nm 纵坐标 荧光染料 PI-DNA复合物 7-AAD 最大激发波长 535 nm 546 nm 最大发射波长 615 nm 647 nm 左下第一象限 活细胞 无荧光 右下第二象限 早期凋亡细胞 绿色荧光 粉红色荧光 橙红色荧光 右上第三象限 晚期凋亡细胞、坏死细胞 红色、绿色双重荧光 红色、粉红色双重荧光 粉红色、橙红色双重荧光 结果图 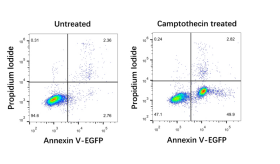
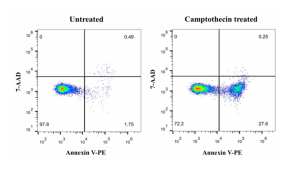
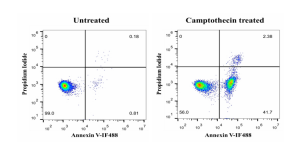
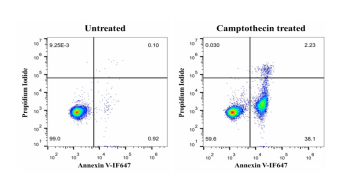
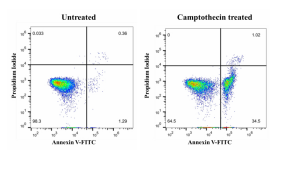
荧光显镜检测
在粘附载玻片(推荐:G6012-1、G6012-2、G6017-20、G6058-20,经过粘附处理,能有效防止组织切片脱落)上加5-10 µL经双染的细胞悬液,
盖上盖玻片,在荧光显微镜下用双色滤光片进行观察,(用荧光显微镜拍照时建议加入适量抗荧光淬灭封片剂(推荐G1401)以防止出现荧光淬灭问题)
试剂盒货号 结果判读 G1510 Annexin V-EGFP呈绿色荧光信号,PI呈红色荧光信号 G1511 Annexin V-FITC呈绿色荧光信号,PI呈红色荧光信号 G1512 Annexin V-PE呈橙红色荧光信号,7-AAD呈粉红色荧光信号 G1513 Annexin V-IF488呈绿色荧光信号,PI呈红色荧光信号 G1514 Annexin V-IF647呈粉色荧光信号,PI呈红色荧光信号
细胞碎片比例过高
可能是由于胰酶消化过度、Annexin V Binding Buffer未正确稀释、细胞状态不佳或实验操作导致的机械损伤。解决方案包括优化胰酶消化步骤、正确稀释Binding Buffer、改善细胞培养条件和温和处理细胞。
空白组有荧光信号
可能原因包括流式细胞仪未清洗干净、细胞不纯或细胞的本底荧光。应重新清洗仪器、鉴定样本纯度和优化细胞培养步骤。
正常细胞出现大量凋亡
可能是由于细胞状态不佳、实验操作导致的损伤或染色时间过长。应调整细胞状态、温和处理细胞和控制实验时间
缺少早期凋亡
可能是由于药物处理不当或药物浓度不适宜。应调整药物处理方式和浓度
缺少晚期凋亡
可能是由于核染料忘记添加或细胞处理条件不适宜。应重新实验并注意添加核染料,以及调整细胞处理条件
分群不明显
可能是由于荧光物质干扰或细胞状态较差。应调整补偿和优化细胞培养
处理组凋亡率过低
可能是由于细胞本身凋亡率低或实验操作问题。应重新优化凋亡诱导实验和收集细胞
实验组中存在斜向上的细胞群
可能是由于荧光染料间的补偿调节不合适。应进行单染管实验以调节补偿
