贴壁细胞
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|---|---|---|---|
| YZ11216-500ML | 22RV1细胞专用培养基 | 125 mL×4 | 350 | |
| YZ10323-500ML | 293A细胞专用培养基 | 125 mL×4 | 350 | |
| YZ10312-500ML | 293T细胞专用培养基 | 125 mL×4 | 350 | |
| YZ10316-500ML | 293细胞专用培养基 | 125 mL×4 | 350 | |
| YZ10317-500ML | 2V6.11细胞专用培养基 | 125 mL×4 | 350 | |
| Y4221-100ML | HEPES solution (1 M) | 100 mL | 80 | |
| Y4061-100ML | 0.02% EDTA细胞消化液(Versene溶液) | 100 mL | 30 | |
| Y1101-50ML | 即用台盼蓝染色液(配套细胞计数仪用) | 50 mL | 80 | |
| Y1030-10ML | 台盼蓝染色液 | 10 mL | 80 | |
| YCP-6DH | 细胞培养板(6孔 爬片 多聚赖氨酸 方形24×24mm) | 1片/袋 | 50 | |
| YCP-6CH | 细胞培养板(6孔 预置细胞爬片 方形24×24mm) | 1片/袋 | 8.5 | |
| YCD-35H | 35mm细胞培养皿(单个装) | 1个/袋 | 0.8 | |
| YCD-60H | 60mm细胞培养皿(单个装) | 1个/袋 | 1.4 | |
| YCD-100H | 100mm细胞培养皿(单个装) | 1个/袋 | 2.4 | |
| YCD-150H | 150mm细胞培养皿(单个装) | 1个/袋 | 5 | |
| YCD-35 | 35mm细胞培养皿 | 20sets/袋 | 16 | |
| YCD-60 | 60mm细胞培养皿 | 10sets/袋 | 9 | |
| YCD-100 | 100mm细胞培养皿 | 10sets/袋 | 14 | |
| YCD-150 | 150mm细胞培养皿 | 5sets/袋 | 25 | |
| YP-1-SF | 1mL 移液管(单支装) | 1mL 100支/袋 | 50 | |
| YP-2-SF | 2mL 移液管(单支装) | 2mL 100支/袋 | 60 | |
| YP-5-SF | 5mL 移液管(单支装) | 5mL 50支/袋 | 35 | |
| YP-10-SF | 10mL 移液管(单支装) | 10mL 50支/袋 | 35 | |
| YP-25-SF | 25mL 移液管(单支装) | 25mL 50支/袋 | 75 | |
| YP-50-SF | 50mL 移液管(单支装) | 50mL 25支/袋 | 75 |
细胞培养是指从动物或植物中取出细胞,然后使其在合适的人工环境中生长。这些细胞可于培养前直接从组织中取出并采用酶或者机械方法进行解离,或者也可用自己经建立的细胞系或细胞株。原代培养是指将细胞从组织中分离后,使其在合适的条件下增殖直到占据所有可用基质(即:达到汇合状态)的培养阶段,在此阶段,必须将细胞转移到新的容器中并更换新鲜培养基,为其提供更多继续生长的空间,从而达到扩大培养的过程,即细胞传代。
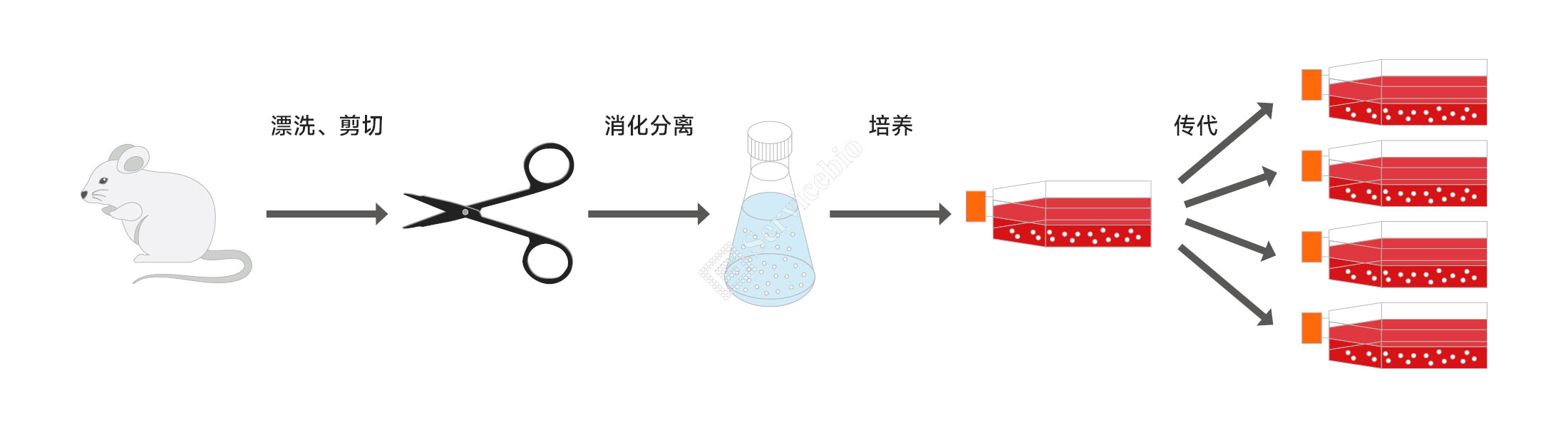
原代培养
1、漂洗、剪切、消化组织:将组织块在平皿中,用不含钙镁的平衡盐溶液,1xPBS缓冲液(G4202-500ML)或DPBS缓冲液(G4200-500ML)冲洗2~3次。组织块剪成3~5mm3大小的小块,剪碎的组织块放入三角瓶中,加入比组织量多30~50倍的0.25%胰蛋白酶消化液(G4021-100ML或G4022-100ML,都含有EDTA)。置于磁力搅拌器SMS-200A上,每隔5~10min轻摇1次,组织块蓬松呈絮状可终止。

2、分离:在消化过程中见消化液浑浊,可用吸管吸取少量消化液在镜下观察,如果组织已经分散成细胞团或单个细胞,立即终止消化,低速离心(500~1000r/min)离心5min(SLX-1024F),去除上清液,采用HBSS缓冲液(G4203-500ML或G4205-500ML)洗2~3min,离心去上清液,共2次,通过适宜的细胞滤网(G6088),滤去尚未充分消化的组织块,低速离心(500~1000r/min)离心5min(SLX-1024F),去上清液,加入一定量的培养液。

3、培养:细胞培养瓶置入37℃培养箱内进行培养
4、维持:初代培养成功,由于营养缺乏,代谢产物增多,细胞未达到饱和密度,仍需继续培养,因此,需采取换液方式来更新营养成分以满足细胞继续生长繁殖的需要。其换液方法比较简单,即弃去旧液,加入与原培养液相同的等量完全培养基。
TIPS:
1、凡经消化处理实体组织来源的细胞要通过充分漂洗,以尽量除去消化液的毒性
2、细胞接种时浓度要稍大,至少为5x10~8个/mL
传代(消化法)
1、漂洗:把原有的细胞培养基吸掉,用不含钙镁的平衡盐溶液,1xPBS缓冲液(G4202-500ML)或DPBS缓冲液(G4200-500ML)冲洗细胞1~2次。(每10cm2培养表面积需要2mL溶液)
2、消化:然后加入适量胰蛋白酶消化液(G4021或G4022,都含有EDTA)。(消化液加入量以能覆盖住细胞为准。)(如果细胞易消化或较脆弱,可选用不含EDTA的胰蛋白酶即G4011和G4013)。25-37℃消化1-5min。37℃,胰蛋白酶消化速度最快。可根据细胞状态调整时间。消化过程可左右摇晃,使消化液与细胞充分接触。
3、终止消化:显微镜下观察,细胞明显收缩,大部分细胞变圆,用移液器轻轻吹吸,能很容易使细胞脱落,表明消化程度合适,用移液器加入4mL完全培养基终止消化。(消化完全的标准:1、 显微镜下观察,细胞明显收缩,且肉眼观察培养器皿底部细胞形态发生明显的变化;2、或用移液器吹打细胞发现细胞刚好可以被吹打下来;此可以时用含血清的培养基 或 胰酶抑制剂终止消化。)
4、悬浮:轻轻吹打细胞,使细胞都悬浮。
5、接种:将培养皿内细胞转移至离心管,离心后去除上清,加入适量该细胞对应的完全培养基,轻轻吹打混匀,然后用台盼蓝进行细胞计数。接着将细胞悬液稀释到该细胞推荐的接种密度,并将适量体积的细胞悬液转移到新的细胞培养容器中(培养皿或培养瓶)。做好标记,放入培养箱继续培养。
TIPS:
1、首先可以在ATCC上查找细胞的传代比例,然后根据细胞培养的状态判断传代的合适比例,若细胞传代过稀则可能会导致细胞不能扩增,若过密则影响细胞生长状态
2、均匀消化,减少细胞团块的形成。
3、吹打过程动作轻柔,避免产生气泡。
4、使用一次性移液管,避免交叉污染,推荐赛维尔移液管(单个装,即开即用,每次用都无菌;滤芯设计,防止污染)。
5、所有与细胞接触的溶液和设备均应为无菌状态,必须采用正确的无菌技术,并且在层流通风厨内工作
1、细胞何时进行传代比较好?
一般情况下细胞生长至完全汇合后就应该传代,所有细胞生长都有一个要求不宜生长过密(也就是常说的长老了),但有接触抑制的细胞,在汇合前就必须进行传代,这类细胞一般在密度70-80%就进行传代,否则会引起细胞分化。
2、CO2培养箱之水盘如何保持清洁?
定期(每周一次)更换水盘里面的水,水盘的水必须使用无菌蒸馏水或无菌去离子,水盘中可添加细胞培养箱用水抑菌剂(G4027-100ML)以预防霉菌污染。
3、细胞离心下来的离心速率应为多少?
细胞传代或冻存时欲回收细胞,其离心速度一般为800-1000 rpm/min,室温离心3-5min,转速过高,将造成细胞破裂死亡。
4、细胞为何生长不均匀?
细胞传代后放入培养箱没有摇匀,或者放入时摇匀,但在细胞贴壁前,又移动了培养瓶,频繁开关培养箱引起的振动或者培养瓶中培养液过少,培养箱搁板表面不平整,这些因素会导致细胞生长不均匀。
5、细胞生长逐渐变慢是什么原因?
1.培养基问题:培养基可能缺乏细胞生长所需的某种因子,或者更换了不同批次的培养基和血清,细胞可能不适应。解决方案是按照细胞库推荐的培养基配方制备培养基,或直接购买细胞专用的培养基,并确保血清和培养基的质量。
2.细胞污染:支原体、细菌、真菌等污染可能导致细胞生长受阻。解决方案是定期检测细胞是否受到污染,并采取相应的抗生素治疗或更换无污染的细胞。
3.细胞密度问题:细胞传代后密度过低,可能会影响细胞生长。解决方案是适当增加细胞接种密度,或将细胞从大培养皿转移到小培养皿中培养。
4.环境因素:温度、湿度、氧气浓度等环境条件不适宜会影响细胞生长。解决方案是优化培养箱条件,确保温度、CO2浓度和pH值等符合细胞生长需求。
5.细胞老化:随着传代次数的增加,细胞可能会逐渐老化,导致生长速度减缓。解决方案是使用较低代数的细胞,或使用永生化的细胞系。
6.消化问题:传代时胰酶消化过度或不足都可能损伤细胞。解决方案是调整胰酶消化的时间和浓度,以确保细胞能够适当分离而不受损。
7.营养物质耗尽:随着细胞生长,培养基中的营养物质可能会被耗尽。解决方案是定期更换新鲜培养液,确保细胞有足够的营养供应。
8.遗传因素:某些基因突变或缺失可能导致细胞生长速度减缓。这种情况可能需要更专业的遗传操作来解决。
9.疾病或损伤:某些疾病或损伤可能会影响细胞的生长速度。解决方案是保持细胞健康,避免物理或化学损伤。
10.药物或化学物质:某些药物或化学物质可能会抑制细胞生长。解决方案是检查培养环境中是否有抑制细胞生长的物质,并将其移除。
