
磁珠法植物RNA提取试剂盒(预封装48T)
- 48 T
磁珠法植物RNA提取试剂盒,适用于从新鲜或超低温冻存的简单植物样本(如水稻叶片、小麦叶片、玉米叶片等)提取高质量RNA,提取的RNA后续可用于RT-YCR、RT-qYCR、Northern杂交、体外翻译、RNase保护分析和分子克隆等等实验,搭配一科Y-48核酸提取仪提取RNA,结果显示:提取的RNA完整性、得率、纯度较好。
产品信息
产品名称 | 产品编号 | 规格 |
磁珠法植物RNA提取试剂盒(预封装48T) | Y3766-48T | 48T |
产品简介
本产品为48T规格预封装板。通过特别优化的裂解缓冲体系,简化了前处理时间,搭配一科Y-16、Y-48核酸提取仪,适用于从新鲜或超低温冻存的植物样本(如叶片、种子、果实、根等)提取高质量RNA。
分离后的RNA下游应用:
RT-YCR
RT-qYCR
mRNA纯化
cDNA文库构建
体外翻译
Northern杂交
特点:
搭配servicebio Y-16、Y-48全自动核酸提取仪进行高通量RNA提取
可替代多步离心步骤
无需有机溶剂
简单便捷的前处理步骤,可在1 h内完成48个样本的同时提取
样本类型与样本量:
30-100 mg新鲜、超低温冻存或组织RNA稳定保存液保存的植物样本(如水稻叶片、小麦叶片、玉米叶片、棉花叶片、大豆叶片、烟草叶片等)
产量:
样本 | 得率 |
本氏烟草叶片(新鲜) | 5-8 µg/80 mg |
玉米叶片(新鲜) | 20-40 µg/80 mg |
水稻叶片(新鲜) | 15-30 µg/80 mg |
油菜叶片(新鲜) | 5-8 µg/80 mg |
陆地棉叶片(新鲜) | 4-7 µg/80 mg |
绿萝叶片(新鲜) | 4-7 µg/80 mg |
银杏叶片(新鲜) | 5-8 µg/80 mg |
绿豆叶片(新鲜) | 30-60 µg/80 mg |
小麦叶片(新鲜) | 30-60 µg/80 mg |
杨树叶片(新鲜) | 20-40 µg/80 mg |
桑树叶片(新鲜) | 30-60 µg/50 mg |
柳树叶片(新鲜) | 20-40 µg/50 mg |
黄豆叶片(新鲜) | 8-15 µg/80 mg |
花生种子 | 30-60 µg/80 mg |
马铃薯块茎 | 1-3 µg/200 mg |
储存与运输
DNase,DTT Solution冰袋(wet ice)运输,-20℃保存;其余试剂室温运输,室温储存;有效期12个月。
组成
Component Number | Component | G3755-48T |
Y3766-1 | Buffer PL1 | 32 mL |
Y3766-2 | DTT Solution | 1.5 mL |
Y3766-3 | DNase | 500 μL |
Y3766-4 | 96孔预封装板 | 3块 |
Y3766-5 | 8孔磁棒套 | 6条 |
说明书 | 1份 | |
使用前准备
1. 检查预封装板是否漏液,如果出现此现象,请勿使用。
2. 使用前观察磁珠或试剂是否粘在封口膜或预封装板孔壁上,如有此现象可上下混匀后短暂离心或于桌面上轻轻敲击预封装板底部至液滴掉落后再使用。
3. Buffer PL1如有沉淀现象,请于65℃加热溶解,待溶解后请向Buffer PL1加入DTT Solution至终浓度为4%,即1 mL Buffer PL1加入40 µL DTT Solution。此裂解液最好现配现用。
4. 使用前向预封装板的第4列和第10列孔位的液体(黄色)中加入10 µL DNase(蓝色),加入DNase后液体为绿色。
操作步骤
1. 植物组织样本裂解:
a. 液氮+研磨仪研磨裂解:提前向2.0 mL Nuclease-free研磨管(推荐YT-200-M)中加入3-4颗4 mm的研磨钢珠(推荐Y0115-200G),取新鲜、超低温冻存或组织RNA稳定保存液(推荐Y3030)保存的植物组织30-200 mg(叶片样本剪碎至0.5 cm2,根、茎和果实剪碎至米粒大小),迅速转移至研磨管中并放到液氮中预冷,将研磨管置于研磨仪(推荐YWE-3D)中进行研磨(放置研磨管前将适配器于液氮中迅速预冷,推荐研磨程序:频率70 HZ,温度-10℃,研磨30 s,取出整个放置样本管的金属适配器,于液氮中遇冷,再次研磨),直至研磨成粉末状。加入600 μL 65℃预热的 Buffer PL1(使用前请确认已加入DTT Solution),涡旋混匀(如果样品研磨不彻底,此时也可再次放到研磨仪研磨),65℃孵育5 min,每隔2 min颠倒混匀一次。
b. 液氮+研钵研磨裂解:取新鲜、超低温冻存或组织RNA稳定保存液(推荐Y3030)保存的植物组织(叶片样本剪碎至0.5 cm2,根、茎和果实剪碎至米粒大小),迅速转移到用液氮预冷的研钵中,加入液氮,研磨组织,其间不断加入液氮,直至研磨成粉末状。称取30-200 mg研磨成粉末的样本到1.5 mL Nuclease-free离心管中,加入600 μL 65℃预热的 Buffer PL1(使用前请确认已加入DTT Solution),涡旋混匀,65℃孵育5 min,每隔2 min颠倒混匀一次;
2. 12,000 rpm,室温离心1 min,将上清转移至一新的1.5 mL离心管中;
3. 重复步骤2;
4. 预封装板准备:取出预封装板,于孔板离心机500 rpm离心1 min或于桌面上轻轻敲击预封装板底部至液滴掉落后再小心撕去封口膜;
5. 向预封装板的第4列和第10列孔位的液体(黄色)中加入10 µL DNase(蓝色),加入DNase后液体为绿色;
6. 转移480 μL步骤3的上清转移至预封装板的第1列和第7列孔位(吸取少量沉淀不会影响提取效果,不足480 μL则将上清全部转移);
7. 将预封装板置于核酸提取仪相应的板位上;
8. servicebio Y-16、Y-48全自动核酸提取仪参数设置:
步骤 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
工位 | 3 | 1 | 2 | 3 | 4 | 3 | 5 | 6 | 5 |
等待时间 | 00:00:00 | 00:00:00 | 00:00:00 | 00:00:00 | 00:03:00 | 00:00:00 | 00:00:00 | 00:03:00 | 00:00:00 |
混合模式a | 2 | 2 | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
混合时间 | 00:00:10 | 00:05:00 | 00:01:00 | 00:01:00 | 00:10:00 | 00:01:00 | 00:01:00 | 00:05:00 | 00:00:10 |
是否暂停 | Ⓧ | Ⓧ | Ⓧ | Ⓧ | Ⓧ | Ⓧ | Ⓧ | Ⓧ | Ⓧ |
吸磁时间a | 00:00:30 | 00:00:30 | 00:00:30 | 00:00:30 | 00:00:30 | 00:00:30 | 00:00:30 | 00:01:00 | 00:00:00 |
体积(µL) | 600 | 900 | 500 | 600 | 100 | 600 | 600 | 80 | 600 |
温度(℃) | --- | 25.0℃ | --- | --- | --- | --- | --- | --- | --- |
a:如果不使用servicebio Y-16、Y-48全自动核酸提取仪,可根据其他适配本产品的仪器说明书调整吸磁时间和混合模式参数。
9. 安装磁套,运行程序;
10. 自动化提取步骤完成后,将第6列和第12列孔位中的核酸溶液小心转移至新的Nuclease-free离心管中,并于-80℃长期保存。
注意事项
1. 请勿将预封装板倒置。
2. 请勿长时间干燥磁珠,以免影响RNA洗脱效率。
3. 程序结束洗脱孔(第6列和第12列)可能存在磁珠残留,可先将96孔预封装板放在磁力架上再吸取样本,尽量避免吸入磁珠。
4. 如果在加入Buffer PL1后上清液粘稠或程序结束洗脱孔(第6列和第12列)提取的核酸样品呈褐色,可适当降低样本投入量。
5. 实验时穿实验服,戴一次性手套,佩戴口罩,避免讲话,使用Nuclease-free的吸头和离心管避免交叉污染。
产品仅供科研用途,不用于临床诊断!
实验案例
使用Y3766-磁珠法植物RNA提取试剂盒(预封装48T)搭配搭配servicebio Y-48核酸提取仪提取16种植物样本RNA,结果显示(图1、表1):16种植物样本提取的RNA浓度、纯度、完整性较好。
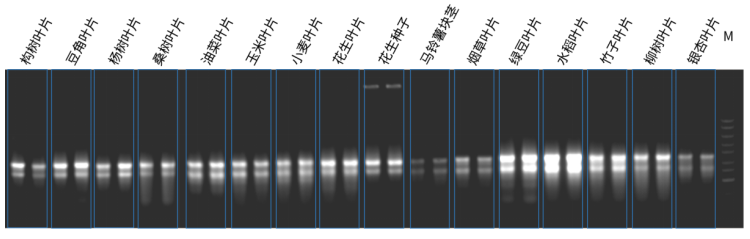
图1:提取16种植物叶片RNA后进行电泳,M:GN8K DNA Marker。
表1:提取16种植物叶片RNA后进行用NanoDrop One检测浓度与纯度
植物材料 | RNA得率 | A260/A280 | A260/A230 |
构树叶片 | 80 µg/50 mg | 2.036 | 1.858 |
2.073 | 2.047 | ||
豆角叶片 | 160 µg/80 mg | 2.05 | 1.84 |
2.072 | 1.897 | ||
杨树叶片 | 48 µg/50 mg | 2.113 | 2.159 |
2.112 | 2.16 | ||
桑树叶片 | 64 µg/50 mg | 2.042 | 1.994 |
2.112 | 2.16 | ||
油菜叶片 | 8 µg/80 mg | 2.046 | 1.959 |
2.067 | 1.995 | ||
玉米叶片 | 24 µg/50 mg | 2.044 | 2.081 |
2.054 | 2.088 | ||
小麦叶片 | 48 µg/80 mg | 2.084 | 2.145 |
2.056 | 2.127 | ||
花生叶片 | 48 µg/80 mg | 2.063 | 2.186 |
2.102 | 2.202 | ||
花生种子 | 120 µg/80 mg | 2.075 | 2.094 |
2.085 | 2.113 | ||
马铃薯块茎 | 3.2 µg/200 mg | 1.859 | 1.173 |
1.893 | 1.246 | ||
烟草叶片 | 8 µg/80 mg | 1.974 | 1.266 |
1.966 | 1.206 | ||
绿豆叶片 | 160 µg/80 mg | 2.079 | 1.918 |
2.089 | 1.989 | ||
水稻叶片 | 32 µg/80 mg | 2.059 | 1.934 |
2.056 | 1.96 | ||
竹子叶片 | 48 µg/80 mg | 2.042 | 2.027 |
2.04 | 2.003 | ||
柳树叶片 | 40 µg/50 mg | 2.045 | 1.959 |
2.084 | 1.948 | ||
银杏叶片 | 8 µg/100 mg | 1.744 | 0.691 |
1.789 | 0.822 |
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|




