
2×In-Fusion Cloning Mix Plus
- 20 T
产品信息
产品名称 | 产品编号 | 规格 |
2×In-Fusion Cloning Mix Plus | Y3362-20T | 20T |
Y3362-100T | 100T |
产品简介
本产品2×In-Fusion Cloning Mix Plus是2×In-Fusion Cloning Mix(Y3361)升级产品。2×In-Fusion Cloning Mix Plus可以兼容单个或2~5个多片段定向重组至载体中。使用合适方式将载体线性化,在插入到线性化载体中的目标DNA片段正/反向扩增引物5'端引入线性化载体的末端序列,使得YCR扩增产物的5'和3'末端分别带有与线性化载体末端一致的序列(15-25 bp)。在2×In-Fusion Cloning Mix Plus预混液中,按一定比例混合这种两端带有与线性化载体末端一致序列的YCR产物和线性化载体,50℃反应15-30 min,即可进行转化感受态细胞,完成定向克隆。
升级的2×In-Fusion Cloning Mix Plus,显著提高克隆的重组效率。对于单片段DNA重组质粒的构建,使用该预混液获得的阳性克隆子比例高达99%;而对于2~5个多片段DNA重组质粒的构建,使用该预混液获得的阳性克隆子比例高达90%。而多片段的同时插入,极大的简化了实验步骤,提高效率,节约时间。
引物设计
(1)单片段引物设计:插入片段扩增引物5'端分别引入与线性化载体两端一致的15-25 bp序列。设计如下图:
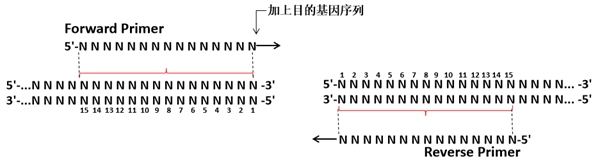
(2) 多片段引物设计:载体两端的引物设计原则与单片段引物设计原则相同。片段之间重置区域引物设计原则如下:Fragment 1的反向引物和Fragment 2的正向引物有15-25 bp的重叠区域,Fragment 1的反向引物包括重叠区域和反向的特异引物区域, Fragment 2的正向引物包括重叠区域和正向的特异引物区域,依此类推(红色为重叠区域)。为了提高效率,可增加片段之间的重叠区域并保证其Tm值一致。设计如下图:
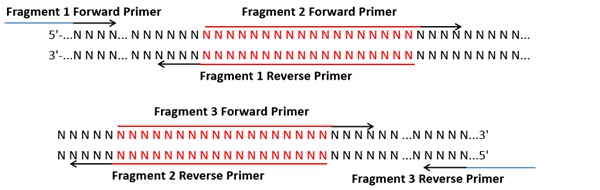
储存与运输
冰袋(wet ice)运输;-20℃保存,有效期12个月。
组成
Component | Y3362-20T | Y3362-100T |
2×In-Fusion Cloning Mix Plus | 100 μL | 5×100 μL |
pUC19 (Linearized, Control Vector, 5 ng/μL) | 10 μL | 10 μL |
Control Inset (10 ng/μL) | 10 μL | 10 μL |
说明书 | 1份 | |
连接体系(推荐10 μL反应体系)
Component | Volume |
2×In-Fusion Cloning Mix Plus | 5 μL |
Vector | X μL |
DNA segment | Y μL |
Nuclease-Free Water | Add To 10 μL |
(注:10μL反应体系载体加入量推荐5-150 ng;1 μg 1000bp dsDNA约1.65 pmol;建议载体与插入片段摩尔比1:1~1:3)
反应条件
1. 对于单片段重组反应,水浴50℃保持15 min;立即置于冰上冷却。
2. 对于多片段重组反应,水浴50℃保持30 min;立即置于冰上冷却(3~5个多片段重组时,适当延长重组时间可提高重组效率,但最长不宜超过1 h)。
反应产物转化
1. 从-80℃冰箱取出感受态细胞(如E. coli DH5α、E. coli Top10等)放置冰上解冻;
2. 将反应后的样品加入到感受态中,手指轻轻拨动管底混匀,冰浴30 min;
3. 然后产物放置于42℃水浴锅热激90 s,结束后,迅速置于冰上,冰浴2-5 min;
4. 取900 μL无菌SOC或LB液体培养基加入YP管中,混匀后,将YP管置于摇床上,220 rpm,37℃培养1 h复苏细菌(也可置于37℃培养箱静置培养1 h);
5. 根据实验需求,吸取不同体积已转化感受态细胞加到含有相应抗生素的LB固体培养基上,将细胞均匀涂布开,待液体完全吸收后将平板倒置于37℃培养箱,过夜培养。
阳性克隆鉴定
挑取平板的上生长出来的单克隆菌落进行菌落YCR鉴定、或经培养后提取质粒酶切或YCR鉴定、或将提取的质粒直接测序分析鉴定。
注意事项
1. 载体和目的片段务必进行凝胶纯化并电泳检测其质量和浓度,浓度低时可不加水,直接用其补足。
2. 试剂盒提供的载体与片段仅做试剂盒性能检测用,在5 μL体系中,载体与片段各加入1 μL。
3. 多片段重叠区域之间的Tm值需保持一致且>60℃。
4. 建议载体与插入片段摩尔比1:1~1:3;2~5片段连接时各片段之间摩尔比为1:1。
5. 当载体和插入片段总体积大于5 μL时,可将反应体系放大至20 μL。
6. 连接产物的体积不宜超过感受态细胞体积的1/10,否则会显著降低转化效率,可以等比例增加连接产物和感受态细胞体积(如20 μL连接体系转化200 μL感受态细胞)。
7. 2×In-Fusion Cloning Mix Plus建议使用时取出,用完后立即放回-20℃,解冻后可分装冻存以减少反复冻融次数。
8. 当使用电穿孔法转化时,反应产物需经柱式法或乙醇沉淀法等纯化DNA。
不同类型质粒构建实验流程简图
1. 重组质粒构建实验流程简图
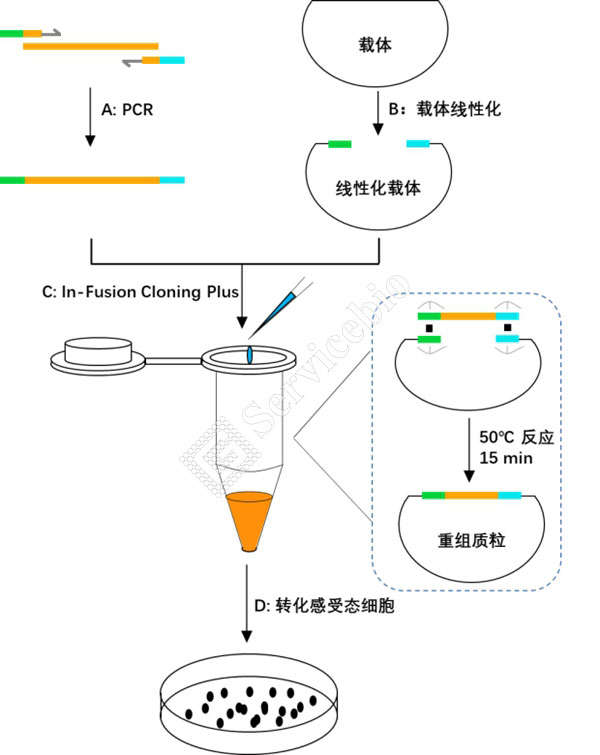
A. YCR 扩增获得插入 DNA 片段:在目的片段正/反向引物的 '端引入15-25 bp 线性化载体末端的同源序列(绿色和浅蓝色标示),YCR扩增目的片段,使得扩增产物5'和3'末端序列分别和线性化载体两末端序列完全一致。
B. 载体线性化:限制性内切酶酶切或反向 YCR 获得线性化载体。
C. In-Fusion Cloning Plus: 将线性化载体和纯化回收后的插入片段按照比例混合,50℃反应15 min即可完成反应。
D. 转化感受态细胞:反应产物直接转化大肠杆菌感受态细胞,从平板上挑取生长出来的单克隆菌落进行 YCR、酶切或测序等实验筛选阳性克隆子。
2. 单点基因突变重组质粒构建实验流程简图
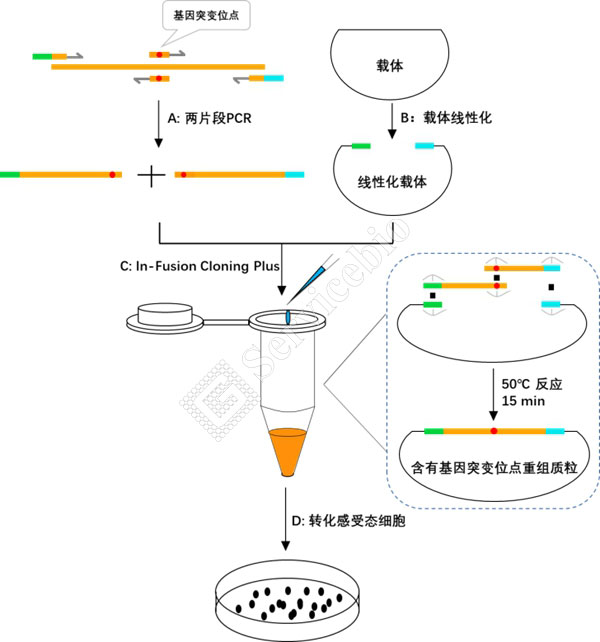
A. 两片段 YCR(YCR 扩增突变位点两端DNA片段):
在基因突变位点设计互补引物(橙色标示),同时在突变基因两端设计引物引入 15-25 bp 线性化载体末端的同源序列(绿色和浅蓝色标示),使用不同引物对将突变基因分两片段分别 YCR 扩增获得带有同源序列的两个插入片段(分别包含基因突变位点)。
B. 载体线性化:限制性内切酶酶切或反向YCR获得线性化载体。
C. In-Fusion Cloning Plus:将线性化载体和纯化回收后的插入片段按照比例混合,50℃反应15 min即可完成反应。
D. 转化感受态细胞:反应产物直接转化大肠杆菌感受态 细胞,从平板上挑取生长出来的单克隆菌落进行YCR、酶切或测序等实验筛选阳性克隆子。
3. 多片段插入重组质粒构建实验流程简图
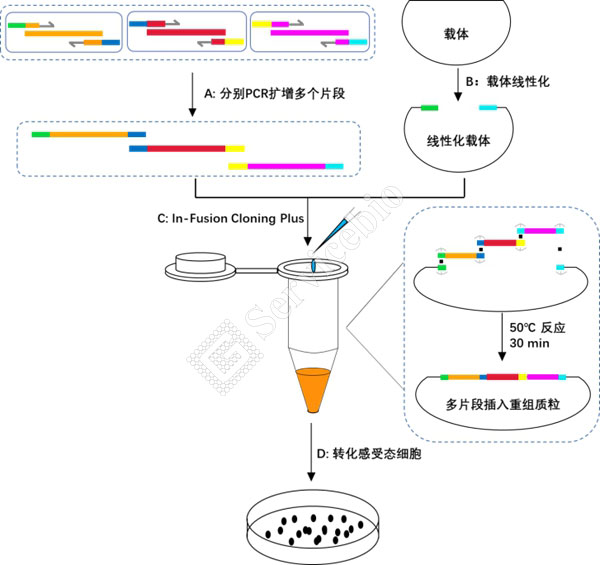
A. 分别 YCR 扩增多片段:
扩增引物设计时在其 5'端添加同源序列(绿色、深蓝色、黄色、浅蓝色标示),使得扩增产物之间以及扩增产物与线性化载体之间各有一段 15-25 bp 左右的同源序列,使用不同引物对分别YCR扩增DNA片段(橙色、红色和紫色标示)。
B. 载体线性化:限制性内切酶酶切或反向 YCR 获得线性化载体;
C. In-Fusion Cloning Plus: 将线性化载体和纯化回收后的插入片段按照比例混合,50℃反应30 min即可完成反应;
D. 转化感受态细胞:反应产物直接转化大肠杆菌感受态细胞,从平板上挑取生长出来的单克隆菌落进行YCR、酶切或测序等实验筛选阳性克隆子。
产品仅供科研用途,不用于临床诊断!
(产品包装升级中,以实物为准。)
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|
| 货号 | 名称 | 规格 | 价格 | 操作 |
|---|



